fosforesciranje je luminiscencija koja nastaje kada energija opskrbljuje elektromagnetska radijacija, obično ultraljubičasto svjetlo. Izvor energije udara elektron iz an atom iz stanja niže energije u "uzbuđeno" više energetsko stanje; onda elektron oslobađa energiju u obliku vidljivo svjetlo (luminiscencija) kada se vrati u stanje niže energije.
Ključni postupci: fosforescencija
- Fosforescencija je vrsta fotoluminiscencije.
- U fosforescenciji svjetlost apsorbira materijal, posrćujući energetsku razinu elektrona u pobuđeno stanje. Međutim, energija svjetlosti ne podudara se s energijom dopuštenih uzbuđenih stanja, pa se apsorbirane fotografije zaglave u trostrukom stanju. Prijelazi u niže i stabilnije energetsko stanje zahtijevaju vrijeme, ali kad se pojave, svjetlost se oslobađa. Budući da se ovo oslobađanje događa polako, čini se da fosforescentni materijal svijetli u mraku.
- Primjeri fosforescentnih materijala uključuju sjaje u mraku, neke sigurnosne znakove i užarenu boju. Za razliku od fosforescentnih proizvoda, fluorescentni pigmenti prestaju svijetliti nakon uklanjanja izvora svjetlosti.
- Iako je nazvan po zelenom sjaju elementa fosfora, fosfor zapravo svijetli zbog oksidacije. Nije fosforescentna!
Jednostavno objašnjenje
Fosforescija polako oslobađa pohranjenu energiju tijekom vremena. U osnovi se fosforescentni materijal "puni" izlaganjem svjetlu. Tada se energija pohranjuje neko vrijeme i polako se oslobađa. Kada se energija oslobađa odmah nakon apsorbiranja energije koja se pojavljuje, postupak se zove fluorescencija.
Objašnjenje kvantne mehanike
U fluorescenciji, površina apsorbira i ponovno emitira foton gotovo trenutno (oko 10 nanosekundi). Fotoluminiscencija je brza jer energija apsorbiranih fotona odgovara energetskim stanjima i dopuštenim prijelazima materijala. Fosforescencija traje mnogo duže (milisekunde do dana), jer apsorbirani elektron prelazi u pobuđeno stanje s većom množinom spina. Uzbuđeni elektroni bivaju zarobljeni u trostrukom stanju i mogu samo koristiti "zabranjene" prijelaze da bi se spustili u singletno stanje niže energije. Kvantna mehanika dopušta zabranjeni prijelaz, ali oni nisu kinetički povoljni, pa im treba duže vremena. Ako se apsorbira dovoljno svjetla, pohranjeno i oslobođeno svjetlo postaje dovoljno značajno da bi materijal mogao izgledati "blistati u tamna. "Zbog toga se fosforescentni materijali, poput fluorescentnih materijala, pojavljuju vrlo svijetli pod crnom (ultraljubičastom) svjetlošću. Jablonski dijagram obično se koristi za prikaz razlike između fluorescencije i fosforescencije.
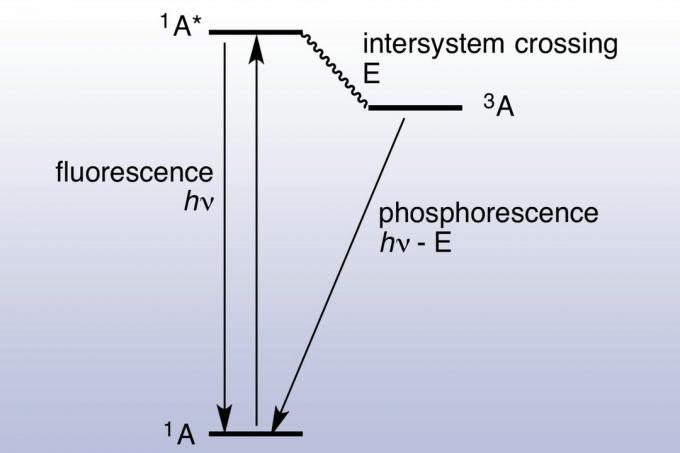
Povijest
Proučavanje fosforescentnih materijala datira iz najmanje 1602. godine kada je Talijan Vincenzo Casciarolo opisao "lapis solaris" (sunčani kamen) ili "lapis lunaris" (kamen od mjeseca). Otkriće je opisano u knjizi profesora filozofije Giulio Cesare la Galla iz 1612. godine De Phenomenis u Orbe Lunae. La Galla izvještava da je Casciarolo kamen propuštao svjetlost nakon što se kalcificirao zagrijavanjem. Dobivala je svjetlost od Sunca i tada je (poput Mjeseca) u tami ispuštala svjetlost. Kamen je bio nečist barit, mada i drugi minerali pokazuju fosforescenciju. Oni uključuju neke dijamant (poznat indijskom kralju Bhoji već 1010.-1055., ponovno ga je otkrio Albertus Magnus i ponovno ga je otkrio Robert Boyle) i bijeli topaz. Kinezi su posebno cijenili vrstu fluorita zvanog klorofan koji bi prikazivao luminiscenciju od tjelesne topline, izloženosti svjetlu ili trljanju. Zanimanje za prirodu fosforescencije i druge vrste luminiscencije na kraju je dovelo do otkrića radioaktivnosti 1896. godine.
materijali
Pored nekoliko prirodnih minerala, fosforescencija se proizvodi i kemijskim spojevima. Vjerojatno najpoznatiji od njih je cink sulfid, koji se u proizvodima koristi od 1930-ih. Cink sulfid obično emitira zelenu fosforescenciju, iako se fosfori mogu dodati da promijene boju svjetlosti. Fosfori apsorbiraju svjetlost koju emitira fosforescencija i potom je oslobađaju kao drugu boju.
U novije vrijeme stroncijev aluminat koristi se za fosforescenciju. Ovaj spoj svijetli deset puta sjajnije od cinkovog sulfida i također dugoročno pohranjuje svoju energiju.
Primjeri fosforescencije
Uobičajeni primjeri fosforescencije uključuju zvijezde koje postavljaju na zidove spavaće sobe koji svijetlu satima nakon što se ugase svjetla i boje koje se koriste za izradu blistavih zvijezdanih freski. Iako element fosfor svijetli zeleno, svjetlost se oslobađa od oksidacije (hemiluminiscencija) i jest ne primjer fosforescencije.
izvori
- Franz, Karl A.; Kehr, Wolfgang G.; Siggel, Alfred; Wieczoreck, Jürgen; Adam, Waldemar (2002). "Luminescentni materijali" u Ullmannova enciklopedija industrijske kemije. Wiley-VCH. Weinheim. doi: 10.1002 / 14356007.a15_519
- Roda, Aldo (2010). Kemiluminiscencija i bioluminiscencija: prošlost, sadašnjost i budućnost. Kraljevsko društvo za kemiju.
- Zitoun, D.; Bernaud, L.; Manteghetti, A. (2009). Mikrovalna sinteza dugotrajnog fosfora. J. Chem. Educ. 86. 72-75. doi: 10.1021 / ed086p72